Was Tie ebenfalls stets betont – und niemand bestreitet: Crispr hat gewaltiges Potenzial. Greift das Tool früh in die DNA eines Embryos ein, wie das Manhattan Genomics plant, sind die Veränderungen später in allen Zellen seines Körpers enthalten. Dazu gehören auch die Zellen der Keimbahn, die Spermien und Eizellen. Das Entfernen einer schädlichen Mutation würde nicht nur das Individuum, sondern auch zukünftige Generationen vor der Krankheit bewahren.
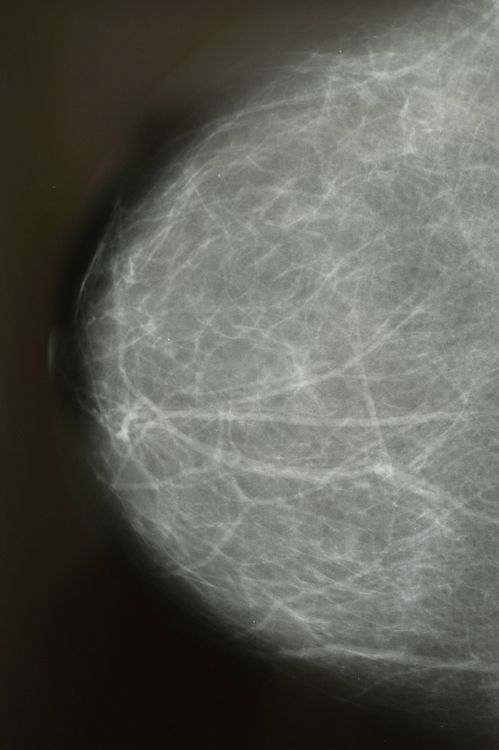
Mit ihrer Firma möchte Tie zunächst schwere Krankheiten angehen, die auf einem einzelnen Gen beruhen. «Davon gibt es sehr viele», sagt sie und nennt Beispiele: zystische Fibrose, Chorea Huntington, Bluterkrankungen wie Sichelzellanämie und erbliche Krebsarten.
Doch die Keimbahn-Editierung ist derzeit fast überall verboten. Nicht nur in europäischen Ländern, auch in den USA oder in China. «Völlig zu Recht», wie der Crispr-Forscher Jacob Corn von der ETH Zürich sagt. «Es gibt noch keine Studie, die zeigt, dass die Methode sicher ist.» Stattdessen belegen Experimente, dass die Crispr-Behandlung von Embryonen zu sogenannten Off-Target-Effekten führen kann: ungewollte Veränderungen, die nicht das Ziel-Gen, sondern andere DNA-Abschnitte betreffen.
Auch bei den chinesischen Designer-Babys sind solche Schäden aufgetreten. Das hat der amerikanische Crispr-Forscher Kiran Musunuru festgestellt, der Zugang zu den Versuchsdaten von He Jiankui hatte. Laut Musunuru erhöhen die Off-Target-Effekte wahrscheinlich das Krebsrisiko der Gen-editierten Kinder.
Erste Therapien, die auf Crispr beruhen
Für Eingriffe in die Keimbahn sei die Wissenschaft noch nicht bereit, sagt Corn. Die Gen-Editierung spezifischer Körperzellen hat aber bereits Einzug in die klinische Praxis gefunden.
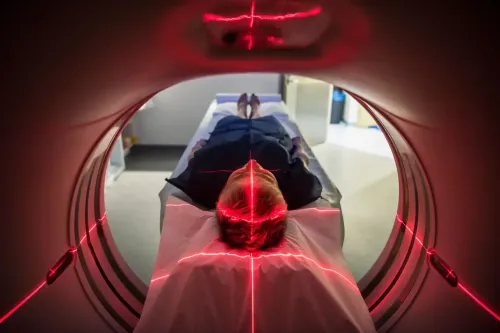
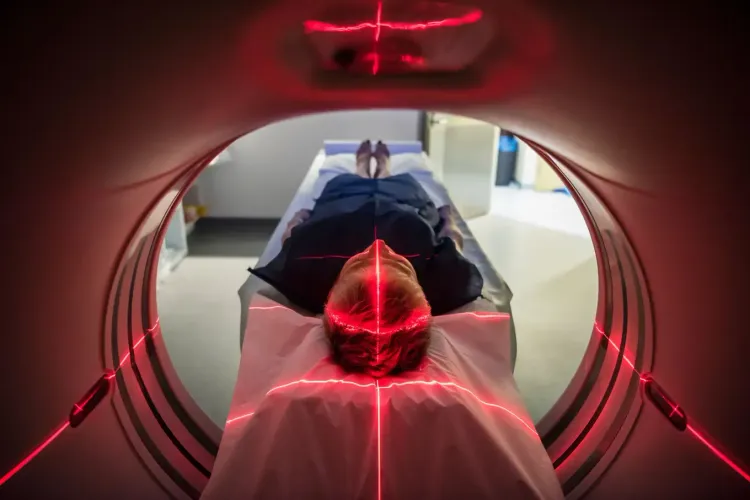
So ist seit 2023 eine auf Crispr basierende Therapie für Jugendliche und Erwachsene mit Sichelzellanämie zugelassen. Und im vergangenen Jahr kam eine noch neuere Methode, das Base-Editing, bei einem Kleinkind mit einer Stoffwechselstörung zum Einsatz: Die massgeschneiderte Behandlung korrigierte die DNA in den Leberzellen. Diese Genveränderungen werden nicht an die nächste Generation weitergegeben.
Solche auf Körperzellen fokussierte Therapien liessen sich auch für viele andere Krankheiten entwickeln, so Corn überzeugt. «Darauf sollte sich die Forschung nun konzentrieren, weniger auf die Keimbahn-Editierung.»
Zudem gibt es bereits heute Optionen für Eltern, die Krankheitsgene in sich tragen. Nutzen sie bei der künstlichen Befruchtung die Präimplantationsdiagnostik, können sie von mehreren Embryonen jene auswählen, die ein intaktes Gen haben. Nur in seltenen Fällen, etwa wenn zu wenige Embryonen vorhanden sind, ist dies nicht möglich.
Gerade hier will Cathy Tie den Eltern zur Seite stehen. «Paare, die eine künstliche Befruchtung versuchen, sind typischerweise eher älter», sagt sie. «Oft haben sie nicht viele Embryonen zur Auswahl.»
Tie findet, die Forschung an der Keimbahn-Editierung sei zu stark eingeschränkt. «Wir wollen zeigen, dass die Methode dank neueren Entwicklungen sicherer geworden ist», sagt sie. Dafür plant ihre Firma vorerst Experimente mit Mäusen, Primaten und menschlichen Zellen. «Hoffentlich können wir die Aufsichtsbehörden dazu bewegen, mehr Forschung in diesem Bereich zuzulassen.» Angesichts der deregulierenden Haltung der Trump-Regierung ist ein solcher Schritt in den nächsten Jahren durchaus möglich.
Langfristig plant Manhattan Genomics eine klinische Anwendung ihres Verfahrens, wie der Reproduktionsmediziner Norbert Gleicher bestätigt, der im wissenschaftlichen Beirat der Firma sitzt. Die gesamte Forschung soll in den USA und in transparenter Weise erfolgen. «Mir wurde versichert, dass keine Versuche im Ausland geplant sind und bereits Kontakt mit den amerikanischen Behörden besteht», sagt er.
Versuche in Ländern mit lascherer Regulation
Die beiden anderen Startups, die Keimbahn-Editierungen in Angriff nehmen wollen, weichen für ihre Experimente dagegen womöglich in Länder mit lascherer Regulation aus. Laut dem «Wall Street Journal» planen Preventive sowie Bootstrap Bio Versuche in Honduras oder in den Vereinigten Arabischen Emiraten.
Der Gründer von Preventive ist der Molekularbiologe Lucas Harrington. Er promovierte im Labor von Jennifer Doudna, die 2020 für ihre bahnbrechende Arbeit zu Crispr den Nobelpreis erhielt. Finanziell unterstützt wird sein Startup von Brian Armstrong, dem CEO der Krypto-Börse Coinbase, sowie vom Ehemann des Open-AI-Chefs Sam Altman. Gründer und CEO von Bootstrap Bio ist der junge Unternehmer Chase Denecke. Von seiner Firma ist wenig bekannt, die Finanzierung legt er nicht offen. Das tut übrigens auch Manhattan Genomics nicht.